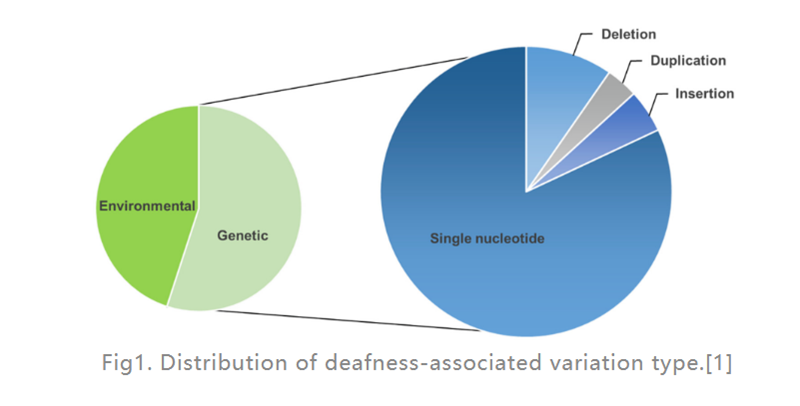
ශ්රවණාබාධ (HL) යනු මිනිසුන් තුළ බහුලව දක්නට ලැබෙන සංවේදී ආබාධිත රෝගයයි.සංවර්ධිත රටවල, ළමුන්ගේ පූර්ව භාෂා බිහිරි භාවයෙන් 80% ක් පමණ ජානමය සාධක නිසා ඇතිවේ.වඩාත් සුලභ වන්නේ තනි-ජාන දෝෂ (රූපය 1 හි පෙන්වා ඇති පරිදි), ජාන විකෘති 124 ක් මිනිසුන්ගේ අසම්මුඛ ශ්රවණාබාධ සමඟ සම්බන්ධ වී ඇති බව සොයාගෙන ඇත, ඉතිරි ඒවා පාරිසරික සාධක නිසා සිදු වේ.දරුණු HL සඳහා ප්රතිකාර කිරීම සඳහා කොක්ලියර් බද්ධ කිරීම (ඇතුළත කණෙහි තැන්පත් කර ඇති විද්යුත් උපාංගයක්) ශ්රවණ ස්නායුවට සෘජුවම ප්රතිකාර කිරීම සඳහා වඩාත් ඵලදායී විකල්පය වන අතර ශ්රවණාධාර (ශබ්ද තරංග පරිවර්තනය කර විස්තාරණය කරන බාහිර ඉලෙක්ට්රොනික උපකරණයක්) මධ්යස්ථ HL සහිත රෝගීන්ට උපකාර කළ හැකිය.කෙසේ වෙතත්, පාරම්පරික HL (GHL) ප්රතිකාර සඳහා දැනට ඖෂධ නොමැත.මෑත වසරවලදී, අභ්යන්තර කණ අක්රියතාවයට ප්රතිකාර කිරීම සඳහා හොඳ ප්රවේශයක් ලෙස ජනක ප්රතිකාරය වැඩි අවධානයක් යොමු කර ඇත.
රූපය1.බිහිරි බව හා සම්බන්ධ විචල්ය වර්ගය බෙදා හැරීම.[1]
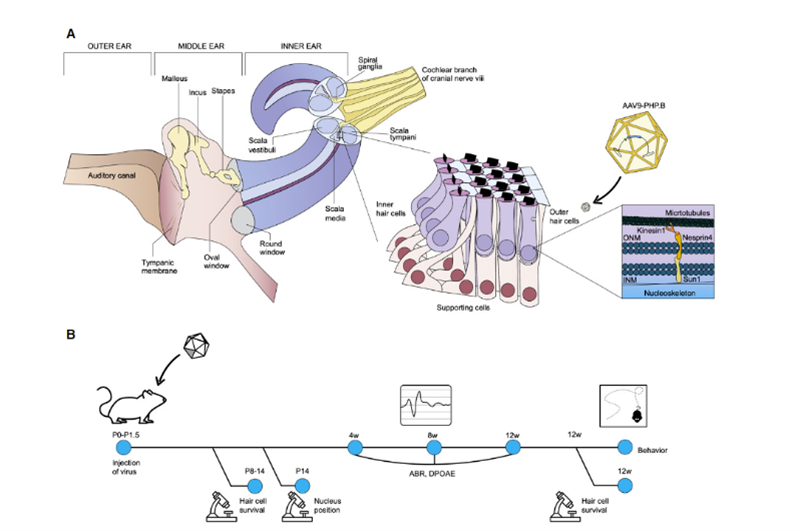
මෑතකදී, සල්ක් ආයතනයේ සහ ෂෙෆීල්ඩ් විශ්ව විද්යාලයේ විද්යාඥයින් විසින් අණුක ප්රතිකාරය - ක්රම සහ සායනික සංවර්ධනය [2] හි පර්යේෂණ ප්රතිඵලයක් ප්රකාශයට පත් කරන ලද අතර, එය පාරම්පරික බිහිරි බව පිළිබඳ vivo ජාන ප්රතිකාර සඳහා පුළුල් යෙදුම් අපේක්ෂාවන් පෙන්නුම් කළේය.සල්ක් ආයතනයේ සහකාර පර්යේෂණ මහාචාර්ය සහ උසස් ජෛව ෆොටෝනික්ස් සඳහා වේට් මධ්යස්ථානයේ අධ්යක්ෂ යූරි මනෝර් පැවසුවේ ඔහු උපතින්ම දරුණු ශ්රවණාබාධයකින් පෙළෙන බවත් ශ්රවණය යථා තත්ත්වයට පත් කිරීම අපූරු තෑග්ගක් බව හැඟෙන බවත්ය.Eps8 යනු ඇක්ටින් බන්ධන සහ ආවරණ ක්රියාකාරකම් සහිත ඇක්ටින් රෙගුලාසි ප්රෝටීනයක් බව ඔහුගේ පෙර පර්යේෂණවලින් සොයාගෙන ඇත;කොක්ලෙයාර් කෙස් සෛල තුළ, MYO15A, WHIRLIN, GPSM2 සහ GNAI3 සමඟ Eps8 විසින් සාදන ලද ප්රෝටීන් සංකීර්ණය ප්රධාන වශයෙන් බොහෝ දුරට පවතී, MYO15A සමඟ එක්ව කෙටි ස්ටීරියෝසිලියා වල ඉඟි වල BAIAP2L2 ස්ථානගත කරන දිගු ස්ටීරියෝසිලියා වල ඉඟි, හිසකෙස් මිටි නඩත්තු කිරීම සඳහා අවශ්ය වේ.එමනිසා, Eps8 හට සාමාන්ය ශ්රවණ ක්රියාකාරිත්වය සඳහා අත්යවශ්ය වන හිසකෙස් සෛලවල ස්ටීරියෝසිලියාවේ දිග නියාමනය කළ හැකිය;Eps8 මකාදැමීම හෝ විකෘති කිරීම කෙටි ස්ටීරියෝසිලියාවට තුඩු දෙනු ඇත, එමඟින් මොළයේ සංජානනය සඳහා ශබ්දය විද්යුත් සංඥා බවට නිසි ලෙස පරිවර්තනය කිරීමට නොහැකි වන අතර එමඟින් බිහිරි භාවයට හේතු වේ..ඒ අතරම, ෂෙෆීල්ඩ් විශ්ව විද්යාලයේ මහාචාර්යවරයෙකු වන සහයෝගිතාකරු වෝල්ටර් මාකෝටි සොයාගත්තේ Eps8 නොමැති විට හිසකෙස් සෛල සාමාන්යයෙන් වර්ධනය විය නොහැකි බවයි.මෙම අධ්යයනයේ දී, මනෝර් සහ මාර්කොටී එක්ව Eps8 ස්ටීරියෝසිලියරි සෛල වලට එකතු කිරීමෙන් ඒවායේ ක්රියාකාරිත්වය යථා තත්ත්වයට පත් කළ හැකිද යන්න සහ මීයන්ගේ ශ්රවණය වැඩි දියුණු කළ හැකිද යන්න විමර්ශනය කිරීමට එක් විය.පර්යේෂක කණ්ඩායම විසින් වටකුරු ජනෙල් පටල එන්නත් කිරීම මගින් Eps8-/- අලුත උපන් P1-P2 මීයන්ගේ කඤ්චුකයට වල් වර්ගයේ EPS8 අඩංගු කේතීකරණ අනුපිළිවෙල ලබා දීම සඳහා ඇඩිනෝ-ආශ්රිත වෛරස් (AAV) දෛශිකය Anc80L65 භාවිතා කරන ලදී;mouse cochlear hair සෛල තුළ stereocilia වල ක්රියාකාරිත්වය පරිණත වීමට පෙර අලුත්වැඩියා කරන ලදී;සහ අලුත්වැඩියා කිරීමේ බලපෑම රූප තාක්ෂණය සහ ස්ටීරියෝසිලියා මැනීම මගින් සංලක්ෂිත විය.ප්රතිඵල පෙන්නුම් කළේ Eps8 ස්ටීරියෝසිලියාවේ දිග වැඩි කර ඇති අතර අඩු සංඛ්යාත සෛලවල කෙස් සෛල ක්රියාකාරිත්වය යථා තත්ත්වයට පත් කළ බවයි.කාලයාගේ ඇවෑමෙන්, මෙම ජාන ප්රතිකාර ක්රමය මඟින් සෛලවලට ගලවා ගැනීමේ හැකියාව නැති වී යන බව ද ඔවුන් සොයා ගත්හ.මීයන් ඉපදීමෙන් පසු Eps8-/- හිසකෙස් සෛල පරිණත වී හෝ අලුත්වැඩියා කළ නොහැකි හානියක් එකතු වී තිබිය හැකි බැවින්, මෙම ප්රතිකාරය ගර්භාෂය තුළ සිදු කිරීමට අවශ්ය විය හැකි බව ය."Eps8 යනු විවිධ ක්රියාකාරකම් සහිත ප්රෝටීනයක් වන අතර ගවේෂණය කිරීමට තව බොහෝ දේ ඇත," මනෝර් පැවසීය.විවිධ සංවර්ධන අවස්ථා වලදී ශ්රවණය යථා තත්ත්වයට පත් කිරීමේදී Eps8 ජාන ප්රතිකාරයේ බලපෑම සහ ප්රතිකාර අවස්ථා දීර්ඝ කිරීමට හැකි වේද යන්න අනාගත පර්යේෂණවලට ඇතුළත් වේ.අහඹු ලෙස, 2020 නොවැම්බරයේදී, ඊශ්රායලයේ ටෙල් අවිව් විශ්වවිද්යාලයේ මහාචාර්ය KarenB Avraham ඔහුගේ ප්රතිඵල EMBO Molecular Medicine [3] සඟරාවේ ප්රකාශයට පත් කර, නව්ය ජාන ප්රතිකාර තාක්ෂණයක් භාවිතයෙන් හානිකර නොවන කෘතිම ඇඩිනෝ-ආශ්රිත වෛරස් AAV9-PHP නිර්මාණය කළේය.B, Syne4-/- මීයන්ගේ රෝම සෛලවල ඇති ජාන දෝෂය, මීයන්ගේ අභ්යන්තර කණ තුළට Syne4 කේතීකරණ අනුපිළිවෙල රැගෙන යන වෛරසයක් එන්නත් කිරීමෙන්, හිසකෙස් සෛල තුළට ඇතුළු වී ගෙන යන ජානමය ද්රව්ය මුදා හරිමින්, පරිණත වීමට සහ සාමාන්ය ලෙස ක්රියා කිරීමට ඉඩ සලසයි (රූපය 2 හි මෙන්).
රූපය2.Corti හි ඉන්ද්රිය සහ nesprin-4 හි සෛලීය ක්රියාකාරිත්වය කෙරෙහි අවධානය යොමු කරමින්, අභ්යන්තර කණ ව්යුහ විද්යාවේ ක්රමානුකූල නිරූපණය.
ප්රතිකාර සඳහා කිසියම් විකෘති ජානයක් ඇතුළත් කිරීම, ඉවත් කිරීම හෝ නිවැරදි කිරීම (එනම් රෝගයේ ජාන වෙනස්වීම් පාලනය කිරීම) මගින් ජාන මට්ටමින් ප්රවේණිගත රෝගවලට ප්රතිකාර කිරීමේ අරමුණ සාක්ෂාත් කර ගැනීම සඳහා ජනක ප්රතිකාර ක්රම භාවිතා කිරීම ඉහළ සායනික බලපෑමක් ඇති බව දැකිය හැකිය.අයදුම් කිරීමේ අපේක්ෂාවන්.ජානමය වශයෙන් අඩු බිහිරි භාවය සඳහා වත්මන් ජාන චිකිත්සක ක්රම පහත දැක්වෙන කාණ්ඩවලට බෙදිය හැකිය:
ජාන විස්ථාපනය
ජාන ප්රතිස්ථාපනය විවාදාත්මක ලෙස ජාන ප්රතිකාරයේ වඩාත්ම “සෘජු” ආකාරය වන අතර එය දෝෂ සහිත ජානයක් හඳුනා ගැනීම සහ ජානයේ සාමාන්ය හෝ වල් ආකාරයේ පිටපතක් සමඟ ප්රතිස්ථාපනය කිරීම මත පදනම් වේ.වෙසිකියුලර් ග්ලූටමේට් ප්රවාහක 3 (VGLUT3) ජානය මකා දැමීමෙන් ඇති වූ ශ්රවණාබාධ සඳහා පළමු සාර්ථක අභ්යන්තර කණ ජාන චිකිත්සක අධ්යයනය;අභ්යන්තර කනේ රෝම සෛලවල (IHCs) බාහිර VGLUT3 අධි ප්රකාශනය AAV1-මධ්යගත බෙදාහැරීම තිරසාර ශ්රවණ ප්රකෘතියක්, අර්ධ රිබන් උපාගමික රූප විද්යාව ප්රතිසාධනය සහ කම්පන සහගත ප්රතිචාර ඇති කරයි [4].කෙසේ වෙතත්, ඉහත හැඳින්වීමෙහි විස්තර කර ඇති AAV- ලබා දුන් ජාන ප්රතිස්ථාපන දෙක ඇතුළු උදාහරණ වලදී, ඇතැම් වර්ගවල ජාන මකාදැමීමේ පාරම්පරික ශ්රවණාබාධ ආබාධ සඳහා භාවිතා කරන මූසික ආකෘති මිනිසුන්ට වඩා තාවකාලිකව වෙනස් වන අතර P1 මීයන් තුළ අභ්යන්තර කණ වර්ධනයේ පරිණත අවධියේ පවතින බව සැලකිල්ලට ගැනීම වැදගත්ය.ඊට හාත්පසින්ම වෙනස්ව, මිනිසුන් උපත ලබන්නේ පරිණත අභ්යන්තර කණකින්.මෙම වෙනස පරිණත මී කන්වලට ජාන ප්රතිකාරය ලබා නොදෙන්නේ නම් මිස මානව පාරම්පරික බිහිරි ආබාධ සඳහා ප්රතිකාර කිරීම සඳහා මූසික ප්රතිඵල යෙදීම වළක්වයි.
ජාන සංස්කරණය: CRISPR/Cas9
“ජාන ප්රතිස්ථාපනය” හා සසඳන විට, ජාන සංස්කරණ තාක්ෂණයේ දියුණුව ප්රවේණික රෝගවලට ප්රතිකාර කිරීමේ ආරම්භය මුල සිටම ගෙන ඇත.වැදගත් ලෙස, ජාන සංස්කරණ ක්රමය ප්රමුඛ පාරම්පරික බිහිරි රෝග සඳහා නොගැලපෙන සාම්ප්රදායික අධි ප්රකාශන ජාන ප්රතිකාර ක්රමවල අඩුපාඩු සහ අධික ලෙස ප්රකාශ කිරීමේ ක්රමය දිගු කාලයක් නොපැවතීමයි.චීන පර්යේෂකයන් විසින් AAV-SaCas9-KKH-Myo6-g2 ජාන සංස්කරණ පද්ධතිය භාවිතා කරමින් Myo6C442Y විකෘති ඇලිලය Myo6WT/C442Y මීයන් විසින් විශේෂයෙන් තට්ටු කිරීමෙන් පසුව, සහ knockout කිරීමෙන් මාස 5 ක් ඇතුළත, මීයන් විසින් ආකෘතියේ ශ්රවණ ක්රියාකාරිත්වය යථා තත්ත්වයට පත් කරන ලදී;ඒ අතරම, අභ්යන්තර කණෙහි හිසකෙස් සෛලවල පැවැත්මේ වේගය වැඩි දියුණු වී ඇති බවත්, සිලියාවේ හැඩය විධිමත් වූ බවත්, විද්යුත් භෞතික විද්යාත්මක දර්ශක නිවැරදි කර ඇති බවත් නිරීක්ෂණය විය [5].Myo6 ජාන විකෘතිය නිසා ඇති වන පාරම්පරික බිහිරි භාවයට ප්රතිකාර කිරීම සඳහා CRISPR/Cas9 තාක්ෂණය භාවිතා කරන ලොව ප්රථම අධ්යයනය මෙය වන අතර එය පාරම්පරික බිහිරි භාවයට ප්රතිකාර කිරීම සඳහා ජාන සංස්කරණ තාක්ෂණයේ වැදගත් පර්යේෂණ ප්රගතියකි.ප්රතිකාරයේ සායනික පරිවර්තනය ස්ථිර විද්යාත්මක පදනමක් සපයයි.
ජාන චිකිත්සාව බෙදා හැරීමේ ක්රම
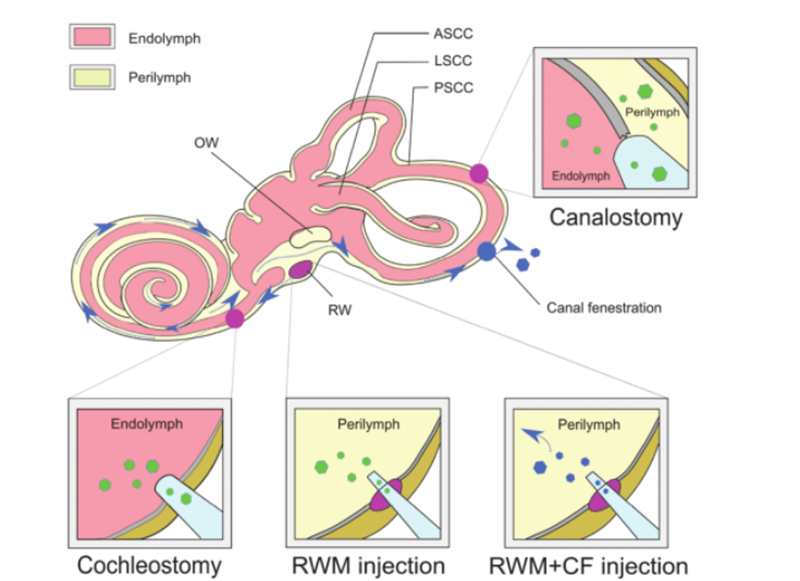
ජනක ප්රතිකාරය සාර්ථක වීමට නම්, නිරුවත් DNA අණු වලට ඒවායේ හයිඩ්රොෆිලිසිටි සහ පොස්පේට් කාණ්ඩවල සෘණ ආරෝපණය හේතුවෙන් සෛල තුලට ඵලදායී ලෙස විනිවිද යාමට නොහැකි වන අතර, පරිපූරක න්යෂ්ටික අම්ල අණුවල අඛණ්ඩතාව සහතික කිරීම සඳහා ආරක්ෂිත සහ ඵලදායී ක්රමයක් තෝරා ගත යුතුය.පරිපූරක DNA ඉලක්කගත සෛලයට හෝ පටකයට ලබාදේ.AAV එහි ඉහළ ආසාදිත බලපෑම, අඩු ප්රතිශක්තිකරණ හැකියාව සහ විවිධ පටක වර්ග සඳහා පුළුල් නිවර්තන හේතුවෙන් රෝග ප්රතිකාර සඳහා බෙදා හැරීමේ වාහනයක් ලෙස බහුලව භාවිතා වේ.වර්තමානයේ, විශාල පර්යේෂණ කාර්යයක් මගින් මූසික කොක්ලියාවේ විවිධ සෛල වර්ගවලට සාපේක්ෂව AAV හි විවිධ උප වර්ගවල නිවර්තන තීරණය කර ඇත.සෛල-විශේෂිත ප්රවර්ධකයින් සමඟ ඒකාබද්ධව AAV බෙදා හැරීමේ ලක්ෂණ භාවිතා කිරීමෙන් සෛල-විශේෂිත ප්රකාශනය ලබා ගත හැකි අතර එමඟින් ඉලක්කගත නොවන බලපෑම් අඩු කළ හැකිය.මීට අමතරව, සාම්ප්රදායික AAV දෛශික සඳහා විකල්පයක් ලෙස, නව කෘතිම AAV දෛශික නිරන්තරයෙන් සංවර්ධනය වෙමින් පවතින අතර අභ්යන්තර කණෙහි උසස් සම්ප්රේෂණ හැකියාව පෙන්නුම් කරයි, ඒවායින් AAV2/Anc80L65 බහුලව භාවිතා වේ.වෛරස් නොවන බෙදාහැරීමේ ක්රම තවදුරටත් භෞතික ක්රම (ක්ෂුද්ර එන්නත් කිරීම සහ විද්යුත් විච්ඡේදනය) සහ රසායනික ක්රම (ලිපිඩ මත පදනම් වූ, පොලිමර් මත පදනම් වූ සහ රන් නැනෝ අංශු) ලෙස බෙදිය හැකිය.පාරම්පරික බිහිරි ආබාධ සඳහා ප්රතිකාර කිරීමේදී ප්රවේශ දෙකම භාවිතා කර ඇති අතර විවිධ වාසි සහ සීමාවන් පෙන්වා ඇත.වාහනයක් ලෙස ජාන චිකිත්සාව සඳහා බෙදා හැරීමේ වාහනයට අමතරව, විවිධ ඉලක්කගත සෛල වර්ග, පරිපාලන මාර්ග සහ චිකිත්සක කාර්යක්ෂමතාව මත පදනම්ව vivo ජාන පරිපාලනය සඳහා විවිධ ප්රවේශයන් භාවිතා කළ හැක.අභ්යන්තර කණෙහි ඇති සංකීර්ණ ව්යුහය නිසා ඉලක්කගත සෛල වෙත ළඟාවීම අපහසු වන අතර ජෙනෝම සංස්කරණ කාරක ව්යාප්තිය මන්දගාමී වේ.පටල සහිත ලිබ්රින්ත් ලෞකික අස්ථියේ අස්ථි ලිබ්රින්ත් තුළ පිහිටා ඇති අතර කර්ණ නාලය, අර්ධ වෘත්තාකාර නාලිකාව, ගර්භාෂ නාලය සහ බැලූනය ඇතුළත් වේ.එහි සාපේක්ෂ හුදකලා වීම, අවම වසා සංසරණය සහ රුධිර වංකගිරි බාධකයක් මගින් රුධිරයෙන් වෙන්වීම, නව ජන්ම මීයන්ට පමණක් ඵලදායී පද්ධතිමය ප්රතිකාර ලබාදීම සීමා කරයි.ජාන චිකිත්සාව සඳහා සුදුසු වෛරස් ටයිටර් ලබා ගැනීම සඳහා, අභ්යන්තර කණ තුළට වෛරස් වාහක සෘජු දේශීය එන්නත් කිරීම අවශ්ය වේ.එන්නත් කිරීමේ ස්ථාපිත මාර්ග ඇතුළත් වේ [6]: (1) වටකුරු කවුළු පටල (RWM), (2) tracheostomy, (3) endolymphatic හෝ perilymphatic cochleostomy, (4) round window membrane plus Tube fenestration (CF) (රූපය 3 හි මෙන්).
රූපය3.ජාන චිකිත්සාව අභ්යන්තර කණ බෙදා හැරීම.
සායනික පරිවර්තන ඉලක්ක මත පදනම්ව ජාන ප්රතිකාරයේ බොහෝ ප්රගතියක් ලබා ඇතත්, ජාන ප්රතිකාරය ප්රවේණි රෝග සහිත රෝගීන් සඳහා ප්රථම පෙළ ප්රතිකාර විකල්පයක් බවට පත් වීමට පෙර, විශේෂයෙන් ආරක්ෂිත සහ ඵලදායී වාහක සහ බෙදා හැරීමේ ක්රමය සංවර්ධනය කිරීමේදී වැඩි වැඩ කොටසක් කළ යුතුව ඇත.නමුත් නුදුරු අනාගතයේ දී මෙම ආකාරයේ ප්රතිකාර පුද්ගලාරෝපිත ප්රතිකාරයේ ප්රධාන අංගයක් බවට පත්වනු ඇති අතර ජානමය ආබාධ සහිත පුද්ගලයින්ගේ සහ ඔවුන්ගේ පවුල්වල ජීවිත කෙරෙහි විශාල ධනාත්මක බලපෑමක් ඇති කරනු ඇතැයි අපි විශ්වාස කරමු.
Foregene විසින් ඉලක්කගත ජාන සඳහා ඉහළ කාර්යක්ෂම පරීක්ෂණ කට්ටලයක් ද දියත් කර ඇත, එය වේගවත් වන අතර RNA නිස්සාරණයකින් තොරව ප්රතිලෝම පිටපත් කිරීම සහ qPCR ප්රතික්රියා සිදු කළ හැකිය.
නිෂ්පාදන සබැඳි
සෛල සෘජු RT-qPCR කට්ටලය - Taqman/SYBR GREEN I
වැඩිදුර නිෂ්පාදන තොරතුරු සඳහා, කරුණාකර සම්බන්ධ වන්න:
පසු කාලය: සැප්-02-2022